Kuidas nimetada keemilisi ühendeid
Autor:
Laura McKinney
Loomise Kuupäev:
2 Aprill 2021
Värskenduse Kuupäev:
26 Juunis 2024

Sisu
- etappidel
- Meetod 1 Ioonsete ühendite nomenklatuur
- Meetod 2 Polüatomiliste ühendite nomenklatuur
- 3. meetod - kovalentsete ühendite nomenklatuur
Keemia valdkonnas edu saavutamiseks on vaja teada, kuidas nimetada peamisi keemilisi ühendeid. Selles juhendis pakutakse teile põhireegleid keemiliste ühendite nimetamisprotsessi kohta ja selle kohta, kuidas määrata teile võõrastele ühenditele nimesid.
etappidel
Meetod 1 Ioonsete ühendite nomenklatuur
- Mis on ioonne ühend? Ioonilised ühendid koosnevad metallist ja mittemetallist. Seejärel vaadake elementide perioodilisustabelit, et teada saada, millised kategooriad kuuluvad ühendis esinevate elementide hulka.
-

Vormige nimi. Miski pole lihtsam kui nimetada ioonne ühend kahest elemendist. Ühendi nime esimene osa vastab tõepoolest järelliidet "ure" kandva mittemetalse elemendi nimele, teine aga metallelemendi nimele. On ka erandeid: oksiid, fosfiid, nitriid, sulfiid.- Näide: Al2O3. al2 = Alumiinium; O3 = Hapnik. Nii saab ühendi nimi "alumiiniumoksiid".
-
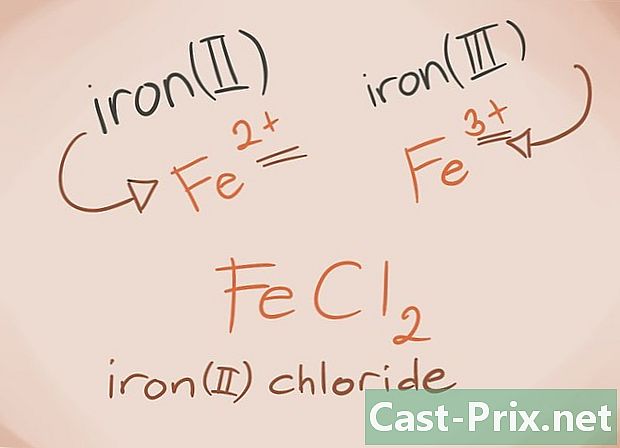
Tunnege siirdemetalle: siirdemetallid on need, mis on toodud perioodilise tabeli D- ja F-plokkides. Ühendi nimel on nende metallide laeng kirjutatud rooma numbritega. Selle põhjuseks on asjaolu, et siirdemetallid võivad kanda rohkem koormust ja moodustada rohkem ühendit.- Näide: FeCl2 ja FeCl3. Fe = raud; Cl2 = -2 kloriid; Cl3 = Kloriid -3. Nimetustena on raud (III) kloriid (II) ja raud (III).
Meetod 2 Polüatomiliste ühendite nomenklatuur
-

Peate mõistma, mis on polüatomne ühend. Polüatomilised ühendid on ühendid, mis on moodustatud üksteisega seotud datomirühma kaudu; kogu laengut kandev rühm on positiivne või negatiivne. Seejärel on kolm põhitoimingut, mida saate polüaatomilistele ühenditele rakendada:- Ühendi esimesele osale võite lisada vesiniku. Sõna "vesinik" on tõepoolest lisatud ühendi nime algusesse. See vähendab negatiivse laengu väärtust ühe võrra. Näiteks "karbonaat" CO3 saab HCO vesinikkarbonaadiks3.

- Samuti saate ühendist hapniku eemaldada. Koormust ei muudeta, kuid ühendi "-ate" järelliide muudetakse "-ique". Näiteks järgmise muutmine: EI3 EI2 me läheme nitraadist nitraadini. "

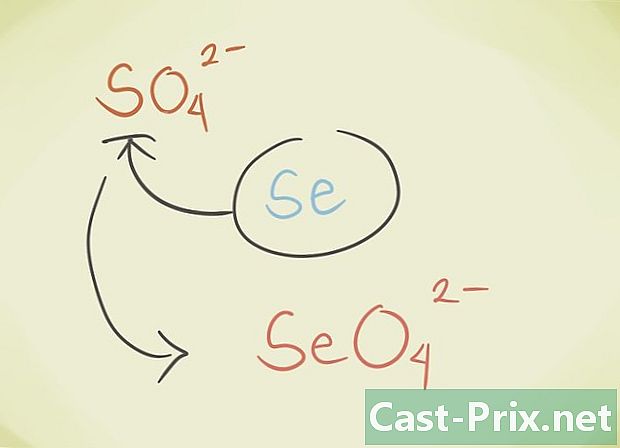
- Võite asendada ühendi kesklatoomi teise aatomiga, mis kuulub samasse perioodilisse rühma. Näiteks SO-sulfaat4 saab asendada Selenate SeO-ga4.
- Ühendi esimesele osale võite lisada vesiniku. Sõna "vesinik" on tõepoolest lisatud ühendi nime algusesse. See vähendab negatiivse laengu väärtust ühe võrra. Näiteks "karbonaat" CO3 saab HCO vesinikkarbonaadiks3.
-

Jäta meelde tavalisemad dioonigrupid. Allpool toodud rühmi kasutatakse enamiku polüatomiliste ühendite moodustamiseks. Pärast nende negatiivse laengu kasvavat järjestust on meil:- hüdroksiidioonid: OH
- nitraatioonid: EI3
- Vesinikkarbonaatioonid: HCO3
- permanganaatioonid: MnO4
- karbonaatioonid: CO3
- kromaadiioonid: CrO4
- dikromaadi ioonid: Cr2O7
- sulfaatioonid: SO4
- sulfitioonid: SO3
- tiosulfaatioonid: S2O3
- Fosfaatioonid: PO4
- ammooniumioonid: NH4
- Vormige liitnimed ülaltoodud loendist. Moodustage rühmaga seotud üksustega nime seos. Kui element asetatakse ioonirühma ette, siis lisatakse elemendi nimi lihtsalt liitnime algusesse.
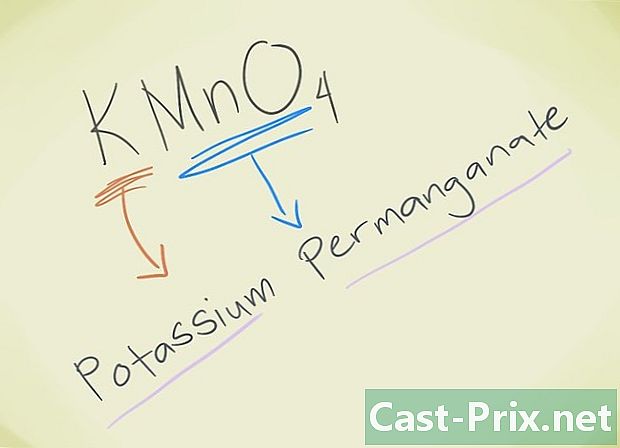
- Näide: KMnO4. Peate saama seda lõvi MnO teada4 vastab lõvipermanganaadile. K tähistab kaaliumi. Nii et teie ühendit hakatakse nimetama permanganate kaaliumiks.
- Näide: NaOH. Tõenäoliselt olete siin juba aru saanud, et see on OHOH. Na on naatrium, seega nimetatakse ühendit naatriumhüdroksiidiks.

- Näide: KMnO4. Peate saama seda lõvi MnO teada4 vastab lõvipermanganaadile. K tähistab kaaliumi. Nii et teie ühendit hakatakse nimetama permanganate kaaliumiks.
3. meetod - kovalentsete ühendite nomenklatuur
-
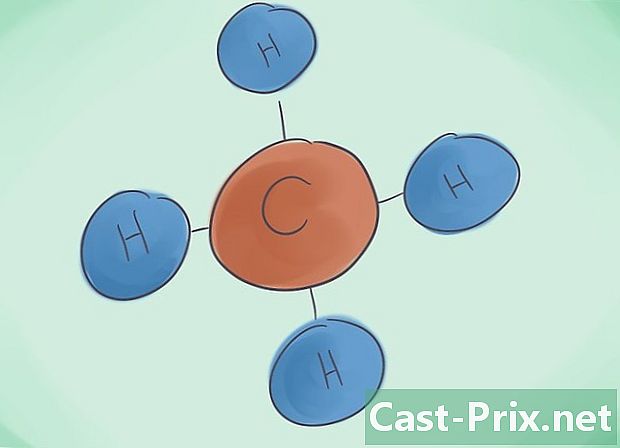
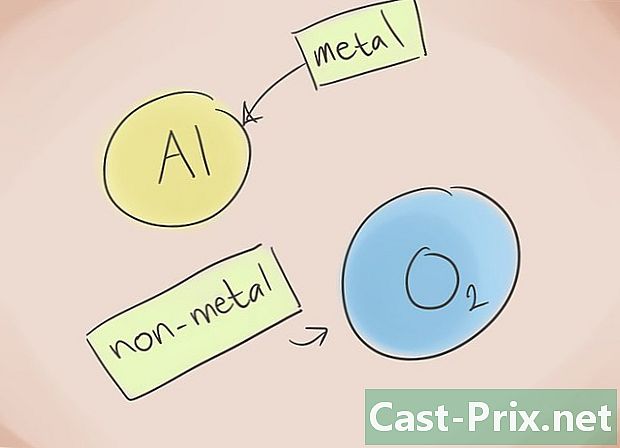
Mis on kovalentne ühend? Kovalentsed ühendid tulenevad vähemalt kahe mittemetallilise elemendi seostumisest. Ühendi nimi määratakse arvandmetega, mis seda moodustavad. Kreeka eesliide selle nime kõrval näitab ühendis esinevate molekulide arvu. -
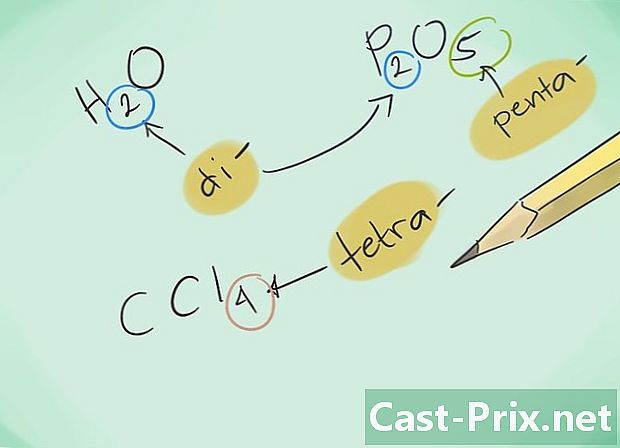
Tutvuge eesliidetega. Pidage meeles 1 kuni 8 aatomiga ühendite järgmised eesliited:- 1 aatom - "mono-"
- 2 aatomit - "Di-"
- 3 aatomit - "tri-"
- 4 aatomit - "tetra"
- 5 aatomit - "Penta-"
- 6 aatomit - "Hexa-"
- 7 aatomit - "Hepta-"
- 8 aatomit - "Okta-"
- Seejärel nimetage ühendid. Pange saadud ühendile nimi, kasutades sobivaid eesliiteid. Prefiksid tuleb pookida igale elemendile, mis koosneb mitme aatomiga ühendist.
- Näide: CO naaseb taas süsinikmonooksiidiks, samal ajal kui CO2 tähistab süsinikdioksiidi.
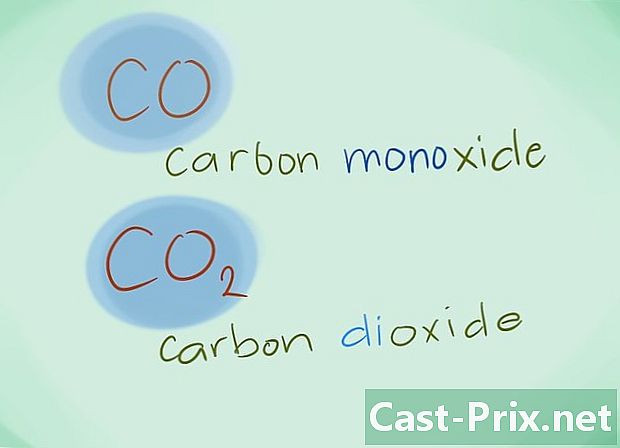
- Näide: N2S3 vastaks lämmastiku trisulfiidile.

- Enamikul juhtudel võib eesliite "mono" ära jätta; see tingib rohkem kui prefiksi puudumise, et viimast tuleks kasutada. Seda eesliidet kasutatakse süsinikmonooksiidi puhul jätkuvalt, arvestades asjaolu, et see kasutus ulatub tagasi keemia esimestesse pilkudesse.
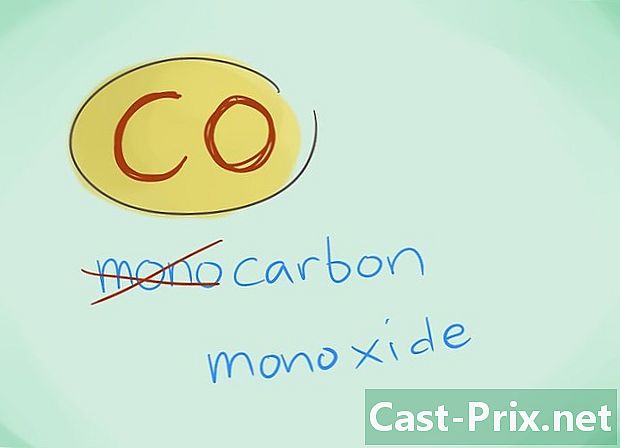
- Näide: CO naaseb taas süsinikmonooksiidiks, samal ajal kui CO2 tähistab süsinikdioksiidi.
- Muidugi kahtlustate, et kõigi nende reeglite suhtes kehtivad mitmed erandid; hoidke näiteks seda valemit, CaCl2Eeldatavasti näete seda nimega "kaltsiumdikloriid", mis on EI. Teie ühend hoiab lihtsalt nime kaltsiumkloriid.
- Samuti tuleb märkida, et see kõik ei kehti orgaanilise keemia kohta.
- Siinsed üksikasjalikud reeglid on mõeldud keemia ja loodusteaduste algajatele. Keemia edasijõudnute etapis on väga erinevad reeglid, näiteks muutuva valentsiga reeglid.

