Kuidas leida oksüdatsiooni numbreid
Sisu
- etappidel
- 1. osa Oksüdatsiooninumbrite määramine keemiareeglite alusel
- 2. osa Määrake aatomite oksüdatsiooninumbrid, mis ei järgi konkreetseid reegleid
Keemias tähistavad terminid "oksüdatsioon" ja "redutseerimine" reaktsioone, milles aatom (või aatomite rühm) kaotab või suurendab vastavalt elektrone. Oksüdatsiooninumbrid on aatomitele (või aatomirühmadele) omistatud numbrid, mis aitavad keemikutel teada, kui palju elektrone saab üle kanda ja kas reaktiiv oksüdeerib või redutseerib reaktsiooni ajal. Protsess, mille käigus aatomitele omistatakse atomiseerimisnumber, võib olla lihtne või väga keeruline, sõltuvalt aatomite laengust ja molekulide keemilisest koostisest, kuhu nad kuuluvad. Asjade täiendavaks komplitseerimiseks võib mõnel aatomil olla rohkem kui kaks oksüdatsiooniarvu. Õnneks reguleerivad oksüdatsiooniarvu määramine täpselt määratletud reegleid, mida on lihtne rakendada, ehkki võib olla kasulik omada teadmisi keemiast ja algebrast.
etappidel
1. osa Oksüdatsiooninumbrite määramine keemiareeglite alusel
-

Tehke kindlaks, kas toode, mille kallal töötate, on elementaarne aatom. Elementaarsete aatomite oksüdatsiooniarv, mis on vabad ja pole teiste elementidega ühendatud, on alati 0. See kehtib aatomite kohta, mille põhivorm koosneb sellest lihtsast aatomist, aga ka nende aatomite puhul, mille elementaarne vorm on diatomiline või polüatomne.- Näiteks Al(S) ja Cl2 mõlemal on oksüdatsiooniarv 0, kuna need on elementaarsel, ühendamata kujul.
- Pange tähele, et väävli algvorm S8või oktaas väävel, ehkki ebaregulaarne, on ka oksüdatsiooniarv 0.
-

Tehke kindlaks, kas kõnealune toode on ioniseeritud kujul. Ioonide oksüdatsiooniarv on võrdne nende laenguga. See kehtib ioonide kohta, mis pole seotud teiste elementidega, aga ka ioonide kohta, mis on ioonse ühendi osa.- Näiteks on Cl iooni oksüdatsiooniarv -1.
- Cl ioon valdab alati oksüdatsiooniarv -1, kui see on osa NaCl ühendist. Kuna Na-iooni laeng on definitsiooni järgi +1, teame, et Cl-iooni laeng on -1. Seega on selle oksüdatsiooniarv alati -1.
-

Metalliioonide puhul võib oksüdatsiooniarvu olla mitu. Paljudel metallielementidel on rohkem kui üks koormus. Näiteks võib raud (Fe) olla ioniseeritud kujul, mille laeng on +2 või +3. Metalliioonide laengud (ja seetõttu nende oksüdatsiooninumbrid) saab määrata ühendi, millesse nad kuuluvad, teiste aatomite laengutest sõltuvalt, või kasutades Rooma numbreid, kui teave on kirjutatud kujul e (nagu lauses: "Raudooni (III) laeng on +3").- Võtke näiteks ühend, mis sisaldab alumiiniummetalliooni. AlCl ühend3 kogulaeng on 0. Teame, et Cl-ioonide laeng on -1 ja ühendis on 3, seega peab Al-iooni laeng olema +3, nii et kogulaeng kõigi ioonide väärtus on võrdne nulliga. Seetõttu on Al oksüdatsiooniarv +3.
-

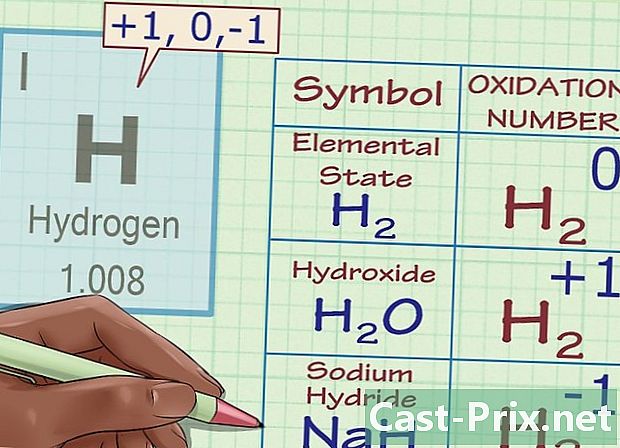
Hapnikule määrake oksüdatsiooniarv -2 (eranditega). sisse kõige rohkem Mõnel juhul on hapnikuaatomite oksüdatsiooniarv -2. Sellest reeglist on siiski mõned erandid:- Kui hapnik on elementaarses olekus (O2), on selle oksüdatsiooniarv 0, nagu kõigi elementaarsete aatomite puhul.
- Kui hapnik on osa a peroksiidi, siis on selle oksüdatsiooniarv -1. Peroksiidid on ühendite klass, millel on lihtne hapniku-hapniku (või peroksiidi anioon) side2). Näiteks H molekulis2O2 (vesinikperoksiid), hapniku (ja selle laengu) oksüdatsiooniarv on -1.
- Kui hapnik on seotud fluoriga, on selle oksüdatsiooniarv +2. Lisateabe saamiseks lugege fluoriidi reegleid sellest artiklist hiljem.
-

Määrake vesiniku oksüdatsiooniarv +1 (eranditega). Hapniku osas on vesiniku oksüdeerimise arv erandjuhtudel. Üldiselt on vesiniku oksüdeerumise arv +1 (välja arvatud juhul, kui see on oma algkujul H2). Spetsiaalsete niinimetatud hübriidühendite puhul on vesiniku oksüdatsiooniarv aga -1.- Näiteks H molekulis2O, me teame, et vesiniku oksüdatsiooniarv on +1, kuna hapniku laeng on -2 ja ühendi kogulaenguks 0 on vaja 2 + 1 laengut.Naatriumhüdroksiidi hübriidvormis NaH on vesiniku oksüdatsiooniarv siiski -1, kuna Na-ioonide laeng on +1; seetõttu, et ühendi kogulaeng oleks null, peab vesinikulaeng (ja seega selle oksüdatsiooniarv) olema võrdne -1.
-

Fluoril on alati oksüdatsiooniarv -1. Nagu me juba mainisime, võib teatud elementide oksüdeerumise arv erineda mitmel põhjusel (see kehtib metalliioonide, peroksiidide hapnikuaatomite jne kohta). Kuid fluori oksüdatsiooniarv on -1 ja see ei muutu kunagi. Selle põhjuseks on asjaolu, et fluor on kõige elektronegatiivsem element - teisisõnu, see on element, millel on kõige vähem võimalust anda üks oma elektronidest, ja see võtab kõige tõenäolisemalt teise elemendi elektron (id). Sellepärast tema laeng ei muutu. -

Vaatleme ühendi oksüdatsiooniarvu võrdsena selle ühendi laenguga. Ühendi kõigi aatomite oksüdatsiooniarvude summa peab olema võrdne selle ühendi laenguga. Näiteks kui ühendit ei laeta, peab selle kõigi aatomite oksüdatsiooninumbrite summa olema 0; kui ühendiks on polüatomiline laenguioon -1, siis peab oksüdatsiooniarvude summa olema -1 jne.- See on hea viis kontrollida, kas olete oma töö hästi teinud - kui teie ühendi oksüdatsiooninumbrite summa ei võrdu teie ühendi kogulaenguga, siis võite olla kindel, et olete teinud vea. kuskil oma oksüdatsiooninumbrite määramisel.
2. osa Määrake aatomite oksüdatsiooninumbrid, mis ei järgi konkreetseid reegleid
-

Leidke aatomid, millel pole oksüdatsiooninumbrite määramise reegleid. Mõne aatomi jaoks pole nende oksüdatsiooniarvu määramiseks spetsiifilisi reegleid. Kui teie aatomit ei kuvata eelmistes lõikudes ja te pole kindel selle laetuses (kui see on näiteks osa suuremast ühendist ja selle individuaalset laengut teile ei anta), siis võite leidke aatomi oksüdeerumise arv kõrvaldamise teel. Esmalt määrake enne ühendi üldise laengu põhjal teile huvipakkuva aatomi arvu kindlakstegemist ühendi kõigi teiste aatomite oksüdatsiooniarv.- Näiteks Na ühendis2SO4, pole väävli (S) laeng teadmata - võime öelda vaid seda, et selle laeng erineb 0-st, kuna see pole oma algkujul. See on hea kandidaat, et rakendada seda algebralist meetodit oksüdatsiooniarvu määramiseks.
-

Leidke ühendi teiste elementide oksüdatsiooninumbrid. Kasutades oksüdatsiooniarvu määramiseks keemilisi reegleid, leia ühendi teiste aatomite oksüdatsiooninumbrid. Pöörake tähelepanu O-, H-aatomite jms erandjuhtudele.- Järgides eelmises osas kirjeldatud keemiareegleid, teame seda Na ühendis2SO4 Na-ioonide laeng (ja seega ka oksüdatsiooniarv) on +1 ja hapnikuaatomite oksüdatsiooniarv on -2.
-

Iga aatomi korral korrutage nende arv oksüdatsiooniarvuga. Nüüd, kui me teame kõigi meie aatomite, välja arvatud huvipakkuva aatomi, oksüdatsiooniarvu, peame arvestama, et mõned neist aatomitest võivad ühendis esineda mitu korda. Korrutage iga aatomi numbriline koefitsient (kirjutatud indeksina ühendis oleva aatomi keemilise sümboli järel) selle oksüdatsiooniarvuga.- Na ühendis2SO4me teame, et seal on 2 Na ja aatomite 4 aatomit. Seega peame tulemuse 2 saamiseks korrutama +1 (Na oksüdeerimise arv) 2-ga, siis korrutama -2 ( O) oksüdeerimine 4-ga, et saada -8.
-
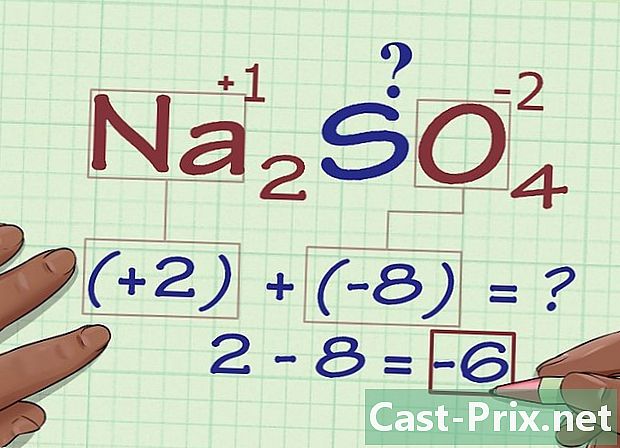
Lisage tulemused. Lisage oksüdatsiooninumbri saamiseks oma korrutuste tulemused ilma arvestage meid huvitava aatomi oksüdeerimise arvuga.- Na näitel2SO4, oleks olnud vaja lisada 2 ja -8, et saada -6.
-
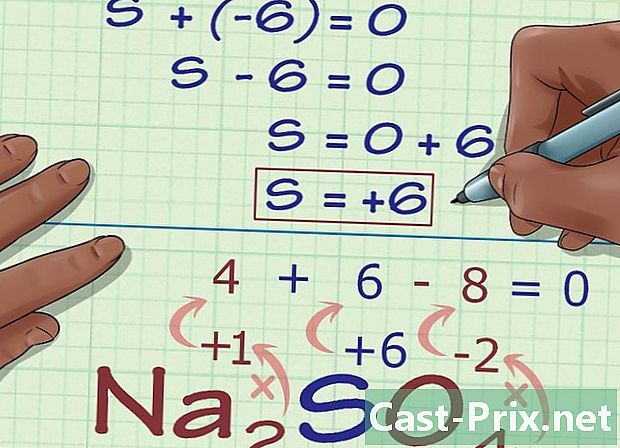
Arvutage tundmatu oksüdatsiooniarv ühendi laengu põhjal. Nüüd on teil kogu teave, mis on vajalik oksüdatsiooninumbri leidmiseks, mis meid huvitab, kasutades lihtsaid algebralisi reegleid. Saate luua võrrandi, mille kohaselt eelnevate etappide tulemused pluss tundmatu oksüdatsiooniarv on võrdsed ühendi üldlaenguga. Teisisõnu: (Teadaolevate oksüdatsiooniarvude summa) + (tundmatu oksüdatsiooniarvu) = (ühendilaeng).- Na näitel2SO4Seda saate teha järgmiselt.
- (Teadaolevate oksüdatsiooniarvude summa) + (tundmatu oksüdatsiooniarvu) = (ühendilaeng)
- -6 + S = 0
- S = 0 + 6
- S = 6. S oksüdatsiooniarv on võrdne 6 Na ühendis2SO4.
- Na näitel2SO4Seda saate teha järgmiselt.

